PEMBENTUKAN DAN SIFAT-SIFAT ASAM KARBOKSILAT
Asam Karboksilat adalah senyawa organik yang mengandung gugus fungsi karboksil. Setelah deprotonasi, asam karboksilat menghasilkan anion karboksilat dengan formula umum R-COO–. Rumus umum asam karboksilat adalah R-COOH, jika COOH merujuk pada gugus karboksil, dan R mengacu pada sisa molekul tempat kelompok ini melekat. Dalam gugus karboksil ini, ada karbon yang berbagi ikatan rangkap dengan atom oksigen dan ikatan tunggal dengan gugus hidroksil.
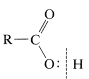
Struktur umum asam karboksilat diilustrasikan di bawah ini.
A. Sifat Fisik
- Molekul asam karboksilat adalah polar karena adanya dua atom oksigen elektronegatif.
- Mereka juga berpartisipasi dalam ikatan hidrogen karena keberadaan gugus karbonil (C = O) dan gugus hidroksil.K
- Ketika ditempatkan dalam pelarut nonpolar, senyawa ini membentuk dimer melalui ikatan hidrogen antara gugus hidroksil dari satu asam karboksilat dan gugus karbonil yang lain.
- Kelarutan senyawa yang mengandung gugus fungsi karboksil dalam air tergantung pada ukuran senyawa. Semakin kecil senyawa (semakin pendek kelompok R), semakin tinggi kelarutannya.T
- Titik didih asam karboksilat umumnya lebih tinggi dari air.
- Senyawa ini memiliki kemampuan untuk menyumbangkan proton dan karena itu asam Bronsted-Lowry.
- Mereka umumnya memiliki bau asam yang kuat. Namun, ester memiliki bau yang menyegarkan dan karenanya digunakan dalam parfum.
B. Sifat Kimia
Sebagian besar reaksi asam karboksilat termasuk dalam salah satu dari empat kelas utama, tergantung pada titik dalam molekul tempat reaksi terjadi.
a. Reaksi yang melibatkan ikatan O − H - ini termasuk disosiasi asam dan reaksi solvolitik.
Contoh :
b. Reaksi pada ikatan karbonil - yang sebagian besar melibatkan serangan oleh nukleofil: N pada karbon karbonil dengan pembelahan ikatan C −. Contohnya adalah esterifikasi, pembentukan asil klorida, dan reduksi dengan hidrida.
Contoh :
Esterifikasi berkataliskan asam dan merupakan reaksi yang reversibel.
c. Dekarboksilasi - ini adalah reaksi di mana ikatan R − C terputus sedemikian rupa sehingga CO2 hilang dan R − H terbentuk. Hampir semua asam karboksilat jika dipanaskan pada suhu tinggi mengalami reaksi dekarboksilasi termal.
Contoh :
d. Substitusi pada kelompok R - penggantian hidrogen atau halogen pada 2-karbon sangat penting.
PEMBUATAN ASAM KARBOKSILAT
Asam karboksilat dapat dibuat melalui beberapa cara :
1. Oksidasi Alkohol Primer dan Aldehida
Pada Reaksi ini, sama-sama menghasilkan asam karboksilat baik itu dalam larutan asam maupun basa. Kekurangan utama dari oksidasi alkohol ialah diperlukannya zat pengoksidasi yang kuat sehingga dalam molekul itu tak boleh ada gugus fungsional yang dapat dioksidasi. Oksidasi aldehida berlangsung dengan zat pengoksidasi lembut (seperti Ag+) yang tidak mengoksidasi gugus lain; namun, aldehida tidak tertsedia semudah alkohol primer.
2. Oksidasi Alkena RCH = HR dan R2C = CHR
Oksidasi alkena yang mengandung satu atom hidrogen pada satu dari atom karbon yang mempunyai ikatan rangkap (=CH–R) dengan oksidator kuat menghasilkan asam karboksilat.
c. Oksidasi gugus alkil pada Cincin Benzena
Seberapapun panjang gugus alkil, akan di degradasi menjadi gugus karboksilat benzoat.
PERMASALAHAN
1. Pada reaksi derkaboksilasi ini, pada saat bereaksi memerlukan suhu yang sangat tinggi. Apabila digunakan pada suhu rendah, Apa yang akan terjadi ? Apakah asam karboksilat masih bisa mengalami reaksi dekarboksilasi ?
2. Mengapa dalam Reaksi Oksidasi Alkohol pada pembuatan asam karboksilat sangat memerlukan zat pengoksidasi yang kuat? sedangkan dalam Reaksi Oksidasi Aldehida malah menggunakan zat pengoksidasi yang lemah.
3. Dalam Reaksi Esterifikasi ini berkataliskan asam. Apabila reaksi ini berkataliskan basa, apakah reaksi ini dapat berlangsung?
REFERENSI














Saya Risa Novalina G (070) akan menjawab permasalahan no 3
ReplyDeleteMenurut saya jika reaksi esterifikasi menggunakan katalis basa itu bisa berlangsung tapi disebut sebagai reaksi transes terifikasi .
Semoga membantu
Assalamualaikum Wafiqah
ReplyDeleteNama saya Firda Oetary (A1C118021) baiklah disini saya akan mencoba menjawab permasalahan no 1. Menurut saya tidak bisa terjadi dekarboksilasi apabila dilakukan pada suhu rendah , karena akan susah mengalami pelepasan gugus karbonilnya .
Terima kasih
Assalamu'alaikum wr wb,baiklah perkenalkan nama saya Nurhalimah disini saya akan menjawab permasalahan yg no 2 dimana permasalahannya yaitu Mengapa dalam Reaksi Oksidasi Alkohol pada pembuatan asam karboksilat sangat memerlukan zat pengoksidasi yang kuat? sedangkan dalam Reaksi Oksidasi Aldehida malah menggunakan zat pengoksidasi yang lemah. Hal tersebut dikarenakan gugus fungsi seperti alkohol hanya dapat di oksidasi oleh oksidasi yg kuat karena alkohol memiliki gugus hidroksil (OH) yang langsung terikat pada atom C sehingga susah untuk dilepas, sedangkan aldehida tidak memiliki gugus hidroksil dia hanya memiliki gugus karbonil dan ada atom hidrogen (H) yg terikat pada atom C.
ReplyDelete